Электронная структура атомов
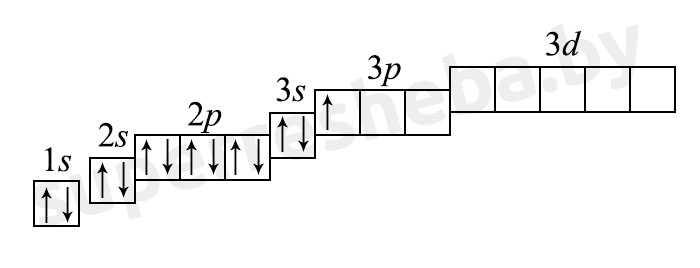
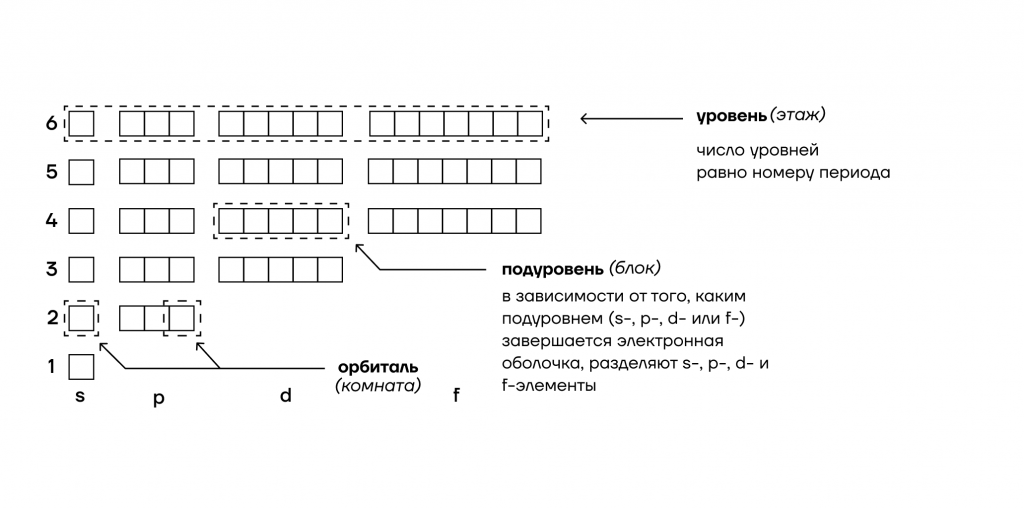
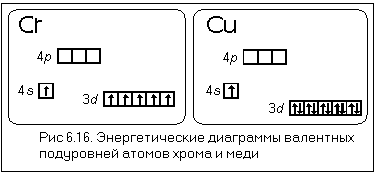
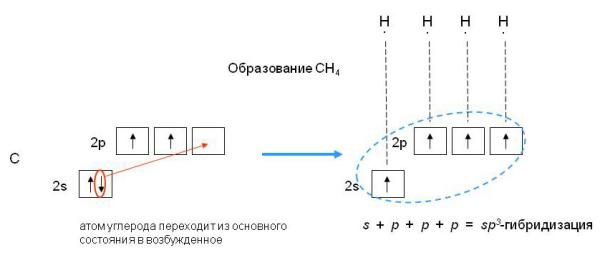
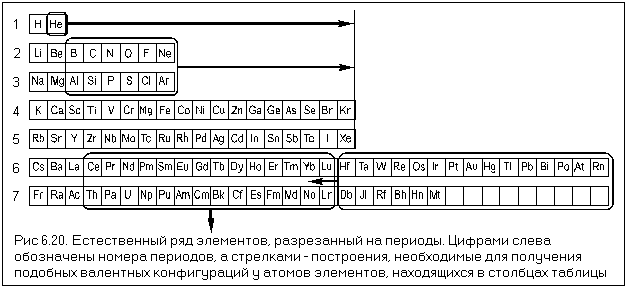
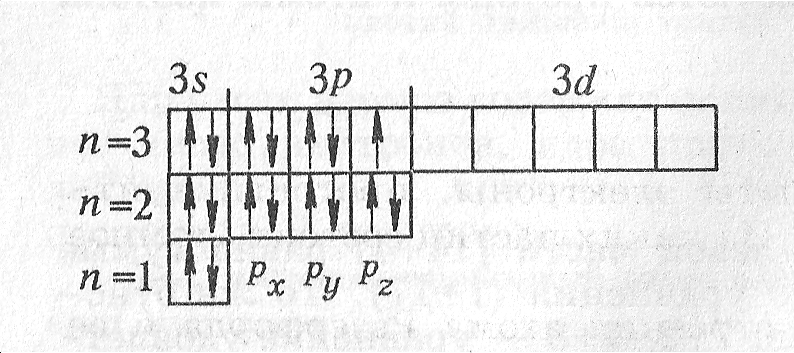
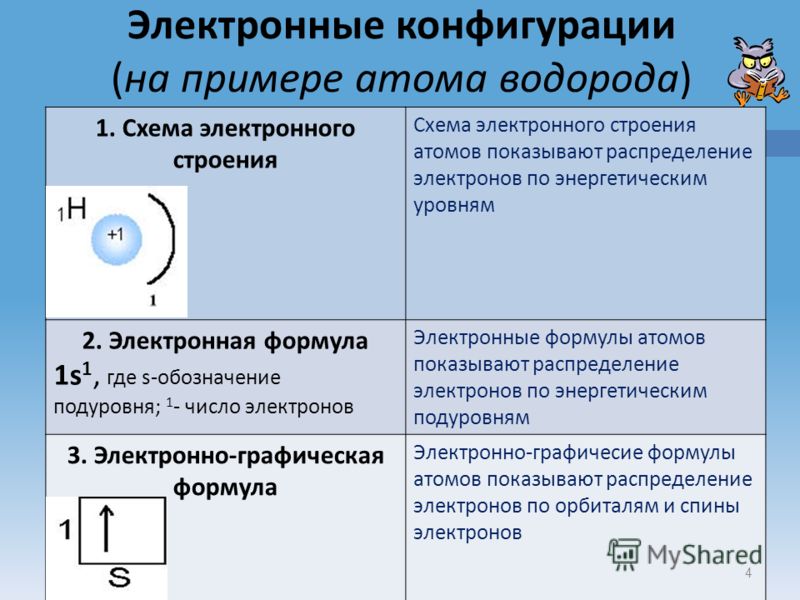
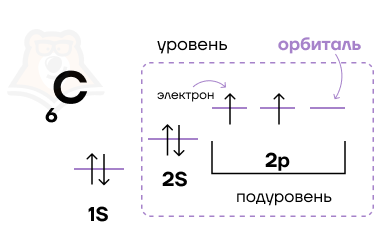
Энергетические уровни и подуровни атома. На рисунке показана диаграмма уровней атома, при помощи которой можно описать электроны любого атома. Энергетические уровни атома электронные облака, образующие электронные атомные слои обозначаются цифрами 1, 2, 3, Энергетические подуровни атома энергетические уровни, характеризующие энергию связи электрона с атомным ядром обозначаются буквами s, p, d, f.







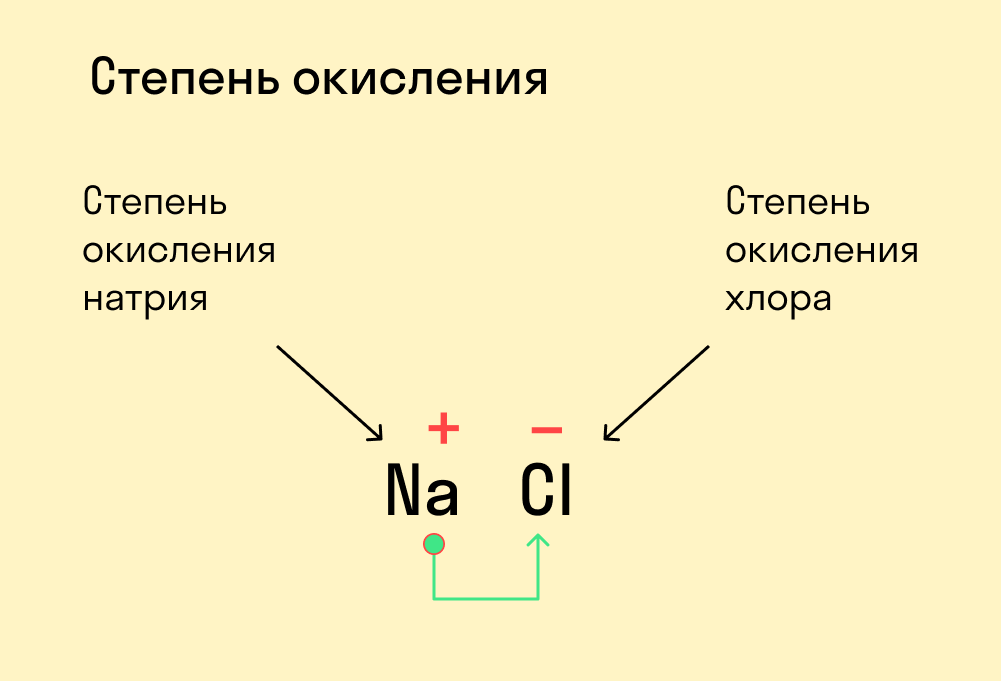
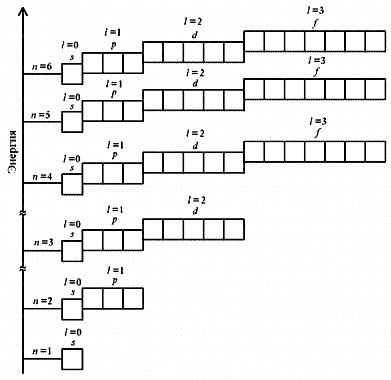
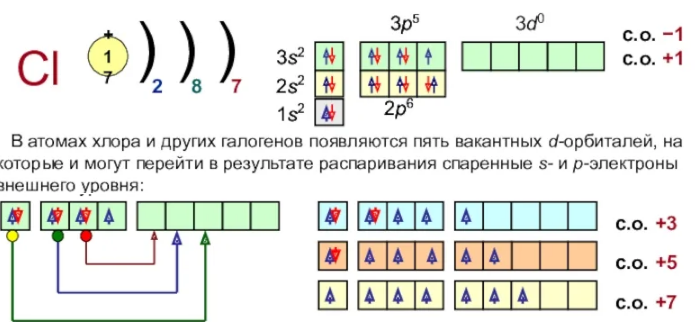
Хлор имеет 17 электронов, заполним электронные оболочки в описанном выше порядке:. Атомы хлора в соединениях имеют степени окисления 6, 5, 4, 3, 2, 1, 0, Степень окисления - это условный заряд атома в соединении: связь в молекуле между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается заряд, то степень окисления отрицательная электроны несут отрицательный заряд , если заряд уменьшается, то степень окисления положительная.



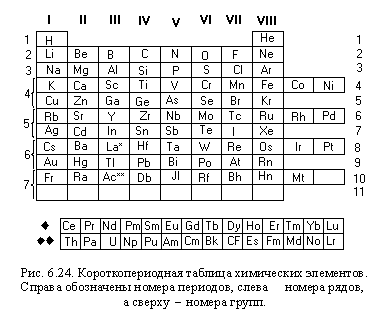
Хлор химический символ — Cl , от др. Chlorum — химический элемент й группы по устаревшей классификации — главной подгруппы седьмой группы, VIIA третьего периода периодической системы химических элементов Д. Менделеева , с атомным номером Простое вещество хлор при нормальных условиях — ядовитый удушающий двухатомный газ формула — Cl 2 желтовато-зелёного цвета, тяжелее воздуха, с резким запахом и сладковатым, «металлическим» вкусом.